| aanadultbraindeath.pdf |
|
Guideline americano para morte encefálica
1 Comment
Procurando por guidelines? Baixe agora esta recente publicação do CDC para prevenção de infeccções relacionada aos cateteres. Para mais informações visite o site oficial do CDC - CLIQUE AQUI. DICA PARA NOSSOS LEITORES: MELHORE A PRONÚNCIA E A COMPREENSÃO DO SEU INGLÊS MÉDICO OUVINDO OS PODCASTS DO CDC
Eli Lilly and Company announced withdrawal of its Xigris® [drotrecogin alfa (activated)] product in all markets following results of the PROWESS-SHOCK study, which showed the study did not meet the primary endpoint of a statistically significant reduction in 28-day, all-cause mortality in patients with septic shock. The company is working with regulatory agencies on this withdrawal, and is in the process of notifying healthcare professionals and clinical trial investigators. Physicians should not initiate treatment with Xigris in new patients and should stop ongoing treatment. The Society of Critical Care Medicine will keep the critical care community updated on this issue as appropriate. More information for clinicians about the withdrawal of activated drotrecogin alfa is available on the European Medicines Agency and the U.S. Food and Drug Administration websites. Adult Update regarding rhAPC Recommendation in Surviving Sepsis Campaign Guidelines* In response to the removal of Xigris® [drotrecogin alfa (activated)], also referred to as rhAPC, in all markets following results of the PROWESS-SHOCK study, the Surviving Sepsis Campaign withdraws its suggestions for use of rhAPC as stated in “Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock.” (1). The study did not meet the primary endpoint of a statistically significant reduction in 28-day, all-cause mortality in patients with septic shock. Eli Lilly and Company, the maker of Xigris ®, is working with regulatory agencies on this withdrawal, and is in the process of notifying healthcare professionals and clinical trial investigators. According to their news release, physicians should not initiate treatment with Xigris in new patients and should stop ongoing treatment. 1. Dellinger RP, Levy MM, Carlet JM, et al. Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock. Crit Care Med 2008; [published correction appears in Crit Care Med 2008; 36:1394-1396] 36:296-327 *This revised recommendation was approved by the Surviving Sepsis Campaign Executive Committee and posted on the SSC website and list-serve on October 27, 2011. Items available below are provided with the intent that they can be printed from this website and used in hospitals across the world to improve patient care. Permission is not granted for commercial use, sales or other purposes not directly related to in hospital clinician education.
CLIQUE NA IMAGEM ABAIXO e conheça o site da campanha sobrevivendo à sepse:
By: JANE S MACNEIL and FLAVIO M OLIVEIRA JR
Risk of death from sepsis increases by 6%-10% with every hour that passes from the onset of septic shock until the start of effective antimicrobial therapy, according to a review of more than 2,600 consecutive cases at 15 intensive care units in five U.S. and Canadian cities in 2005. “You already have a substantially increased risk of death if you get antibiotics by the second hour after onset of hypotension compared with the first hour—and that odds ratio continues to climb out to 36 hours,” principal investigator Anand Kumar, M.D., said at a meeting sponsored by the Society of Critical Care Medicine. Relatively few patients received appropriate antibiotics within 2 hours, however. Dr. Kumar, head of the emergency department at the University of Manitoba in Winnipeg, reported that at every hospital studied, “Only half of septic shock patients received an antibiotic within 6 hours of onset of recurrent or persistent hypotension.” Early administration of appropriate antibiotics is crucial because it eliminates the source of sepsis, according to Dr. Kumar. “You can keep the patients alive for days, but if you don't eliminate the source in the first couple of hours, they are not going to make it,” he said. All told, 43.8% of 2,731 septic shock patients reviewed by Dr. Kumar and his colleagues survived to hospital discharge. Removing patients who were moribund at presentation (those who required intubation or cardiopulmonary resuscitation in the field) reduced the population to 2,675 patients, but barely nudged the survival rate up to 44.7%. The population had slightly more men than women and an average age of 62.5 years. Nearly half the patients, 43%, came from emergency departments. Another 28% had been in medical wards, and 18% on surgical floors. Nosocomial infections accounted for 42% of cases. Malignancy was the most common comorbidity (20%), followed by chemotherapy and elective surgery, each about 15%. The average Acute Physiology and Chronic Health Evaluation II score was 25.9. Dr. Kumar said emergency departments were about an hour faster than other areas of the hospital in delivering antibiotics, but still too slow. The median emergency department time to treat was 4.5-5 hours. The investigation started with animal studies. Mortality was held to 10% if the animals were given an antibiotic within a 12-hour window before the onset of hypotension, according to Dr. Kumar. The mortality was 80% if the antibiotic was started 15 hours afterward, and 100% at 24 hours. In the human retrospective study reported at the meeting, 89% of patients who received an appropriate antibiotic within the first half-hour survived, he said. By the second hour, the survival rate dropped to 84%, and it continued to drop at a rate of 7.5% every hour thereafter. Subset analyses by numerous factors mostly produced P values of .0001 without changing the risk, according to Dr. Kumar. Patients who were obviously sicker at presentation received antibiotics faster, improving their odds of surviving, he said. Only about 50 patients, all in the United States, had methicillin-resistant Staphylococcus aureus, which was not seen in Winnipeg, according to Dr. Kumar. He noted that the investigators focused on time to effective antibiotics. If the first choice is not effective, the effects of any initial delay can be all the more overwhelming, he said. Dr. Kumar called for hospitals to use medical response teams with algorithm protocols for patients in septic shock. He reported his hospital instituted the following changes in response to the study: ▸ Staff can start intravenous antibiotics in hypotensive sepsis patients without waiting for approval. ▸ Nurses have been told that the first dose of any new antibiotic is an automatic stat order. ▸ No sepsis patient is transferred to an ICU without receiving an antibiotic before leaving the emergency department. Many emergency physicians do not realize that an antibiotic order may wait for hours if it is not marked “stat,” according to Dr. Kumar. If the patient is transferred to an ICU, more hours might pass before the antibiotic is delivered with scheduled medications, he warned. “These simple administrative changes can reduce time to antibiotics by 2 hours,” he said. “And, if these data hold, that's a translation to a 15% absolute improvement in mortality.” Com EstudAusculta, você vai ouvir os sons cardíacos e pulmonares típicos da propedêutica clínica associada a um texto super-didático que descreve o som ouvido, além de explorar a etiologia dos distúrbios cárdio-pulmonares.
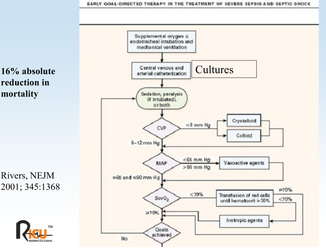
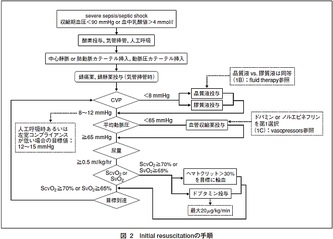
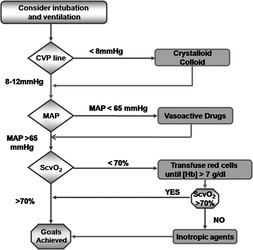
Ausculta cardio-pulmonar Artigos que impactaram positivamente a medicina intensiva nos ultimos anos, conhecidos como must read: EARLY GOAL-DIRECTED THERAPY IN THE TREATMENT OF SEVERE SEPSIS AND SEPTIC SHOCK
Sobre o Autor deste paper: Emanuel Rivers Emanuel Rivers é Vice-Presidente e Diretor de Pesquisa do Departamento de Medicina de Emergência. Ele é médico Senior e Staff na Unidade de Cuidados Críticos e Cirúrgicos do Departamento de Emergência do Hospital Henry Ford em Detroit, Michigan. Recebeu seu Bacharelado em Ciências, Mestrado de Saúde Pública e Doutor em Medicina pela Universidade de Michigan em Ann Arbor, Michigan. Completou sua residência em emergência e medicina interna na Henry Ford Hospital, Detroit, Michigan, seguido por uma bolsa de estudos em medicina de cuidados intensivos da Universidade de Pittsburgh, PA. Atualmente professor Emanuel Rivers é Board Certified em Medicina Intensiva, Medicina de Emergência e Medicina Interna. Ele também tem uma competência especial em Medicina Hiperbárica. Rivers é ganhador do prêmio nacional ou internacional de pesquisa da Sociedade de Medicina de Emergência Acadêmica (2010), American College of Emergency Physicians (2005), Society of Academic Emergency Medicine (2000), American College of Chest Physicians (2000), Society of Critical Care Medicine e Sociedade Europeia de Cuidados Críticos Prêmio de Pesquisa de Medicina (2000). Ele é um membro da Academia Americana de Medicina de Emergência, do American College of Chest Physicians e membro de longa data da Society of Critical Care Medicine. Ele foi o primeiro médico da história do Henry Ford Hospital a ser introduzido no Instituto de Medicina, Academia Nacional de Ciências em 2005 e foi chamado para servir em forças-tarefa e para aconselhar o governo dos Estados Unidos sobre questões de saúde publica. Tambem foi eleito para o Docs Top na cidade de Detroit para os anos de 2006 a 2010. Ele também é consultor de qualidade para três dos dez melhores sistemas de saúde e assistência ao parto nos Estados Unidos. Dentre os interesses de Rivers em pesquisa clinica, destacam-se o exame e tratamento de doença grave ou em estado crítico nos estágios iniciais de apresentação no hospital, que inclui o Departamento de Emergência e Unidade de Terapia Intensiva. Doenças, que estão incluídas nesta área, são os pacientes com choque de todos os tipos (séptico, trauma ou hemorragia, sindromes coronarianas, tromboembolismo venoso, parada cardio-respiratoria. Atualmente Rivers estuda novas maneiras de melhorar a detecção precoce e tratamento agressivo destas doenças, que tem custado muitas vidas no mundo, alem de consumir recursos em cuidados de saúde. Contribuições - O "protocolo de Rivers" O algoritmo de reanimação em emergencia no cenário de sepse grave e / ou choque séptico foi formalmente conceitualizado por Emanuel Rivers em Novembro de 2001 quando criou o "early-goal protocol" ou protocolo de terapia precoce guiada por metas (EGDT), no departamento de emergência. EGDT tem sido utilizado e validado por muitos anos na unidade de cuidados intensivos , mas o papel de Rivers, expandiu a idéia de incorporar todos aqueles pacientes que chegam inicialmente ao departamento de emergencia com sinais de sepse grave ou choque séptico . Muitos hospitais em todo o mundo, inclusive aqui no Brasil, rapidamente incorporaram o protocolo desenvolvido por Rivers em seus algoritmos de tratamento de emergencia. O EGDT também foi citado pela Comissão Conjunta de Acreditação Hospitalar como uma iniciativa de melhoria de qualidade dos servicos prestados. Discussão O estudo EGDT foi uma marco nao apenas para a medicina intensiva, mas para toda a medicina, e um reflexo disso foi que as recomendações deste estudo foram reproduzidas em mais de 33 outras publicações mundo afora, desde 2001 que compreende mais de 8.000 pacientes com igual eficácia e melhoria nos custos dos cuidados de saúde. Rivers não ganhou dinheiro a partir das pesquisas nesta área e não tem relatado conflito de interesses em suas pesquisas. Fonte: wikipedia Gostaria de contactar o prof. Emanuel Rivers? Clique no link abaixo: http://www.docspot.com/user/1246643921 _Empiema / Decorticação Pulmonar
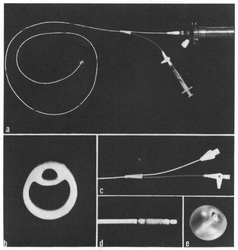
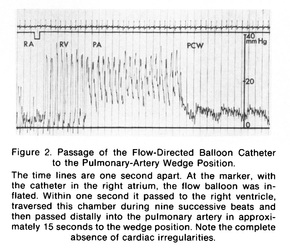
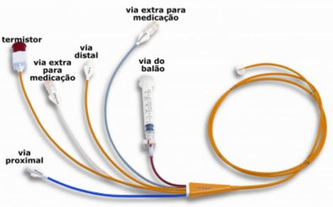
Prof. Fernando Ramos, RN MSc O que é isso? Empiema é a infecção no espaço pleural. O espaço pleural é o espaço potencial entre o pulmão e a parede torácica. O desenvolvimento do empiema e' o resultado da infeccåo do líquido no interior do espaço pleural, e a deposição de material protéico e fibrina, infectados, na superfície do pulmão e da parede torácica. O material infectado depositado sobre o pulmão é chamado de casca pleural. O espaço pleural normalmente tem uma superfície úmida, permitindo que a expansão e contração do pulmão deslize suavemente sobre o interior da parede torácica. Em circunstâncias normais, não há quantidade significativa de fluido no espaço pleural. O pulmão é normalmente completamente expandido dentro do torax. Quando um empiema está presente, o pulmão é comprimido pela presenca do líquido no espaço pleural. O pulmão torna-se "preso" dentro do material, tornando-o incapaz de se expandir. O que causa um empiema pleural? A maioria dos empiemas começa como uma pneumonia. Alguns pacientes com pneumonia desenvolvem derrame pleural parapneumonico. Na maioria dos pacientes, a efusão pleural se resolve quando a pneumonia é tratada. Em alguns pacientes o derrame torna-se infectado. Uma efusão pleural infectada é chamado de empiema. O empiema tem dois componentes: o líquido no espaço, geralmente pus e os depositos fibrinosos - as cascas pleurais depositadas sobre o pulmão e parede torácica. A grande maioria dos empiemas não responde aos antibióticos, os empiemas tambem nao sao auto-limitados, ou seja nao se resolvem por conta própria. A grande maioria requerem exploração cirúrgica e drenagem. (veja o video abaixo) Outras causas de empiema são infecções secundárias distantes associados a um derrame pleural benigno, por exemplo, um paciente com insuficiência cardíaca pode desenvolver um derrame pleural. O mesmo paciente pode desenvolver uma infecção do trato urinário. Bactérias da infecção do trato urinário podem, por via hematogenica, infectar o derrame pleural, resultando em um empiema mais tarde. Uma causa relativamente rara de empiema nos Estados Unidos é a tuberculose. Empiemas tuberculosos estão associados com tuberculose pulmonar, muito mais com que focos distantes. Como é tratado? Na presença de pneumonia, a base do tratamento do empiema é a antibioticoterapia voltada para a propria pneumonia. Em conjunto com os antibióticos, o fluido infectado deve ser drenado, e os debris da "casca pleural" devem ser removidos das paredes do pulmão e do tórax. Se o processo for diagnosticado cedo, um procedimento minimamente invasivo - a toracoscopia (VATS) - pode ser considerado. Através de minúsculas incisões, sob orientação endoscópica, o líquido é drenado e as cascas pleurais removidoas da superfície da parede do pulmão e do tórax. Dois ou três drenos torácicos são deixados no espaço pleural. Eles geralmente são removidos 4 a 7 dias após a cirurgia. Se o processo for descoberto mais tardiamente e a quantidade e densidade da casca pleural exceder a capacidade da toracoscopia em removê-lo, uma toracotomia sera necessária. No momento da toracotomia, uma incisão de aprox. 5 a 6 polegadas é realizada na parede torácica. O fluido infectado é removido e é enviado para análise. A casca é cuidadosamente removida (pleura visceral) do pulmão e (pleura parietal) da parede torácica. O pulmão é novamente re-expandido. Vários drenos poderão ser introduzidos e permanecer no local por 4-7 dias. por Flavio Monteiro e Fernando Ramos Em 1970 os 2 autores acima (Jeremy Swan e William Ganz) publicaram no NEJM um trabalho pioneiro que revolucionou a medicina intensiva. Pela primeira vez foi possível se cateterizar a artéria pulmonar, à beira do leito, de forma segura e com reduzido índice de complicações. O cateter de artéria pulmonar permitiu também um melhor conhecimento da fisiopatologia dos estados agudos de disfunção cardiovascular e choque de qualquer etiologia. O cateter inicial, com apenas dois lúmens, como vocês podem conferir nas imagens acima, é bem diferente dos modernos e multiparamétricos cateteres utilizados atualmente, porém utiliza como base os mesmos princípios do original, que possuía um balão insuflável em sua ponta e por isso era possível introduzi-lo até a artéria pulmonar sem a necesidade de fluoroscopia (laboratório de hemodinâmica comumente usados hoje em dia para cateterização coronariana) para visualizacao direta. Através deste artificio, foi possível aferir-se diretamente a pressão de oclusão da arteria pulmonar (PAOP), uma estimativa da pressão atrial ESQUERDA, pressão de enchimento do atrio esquerdo ou pré-carga atrial esquerda. O trabalho inicial descreveu a passagem do cateter em 37 pacientes criticos e em 33 pacientes submetidos a cateterismo cardiaco, deixando claro que se tratava de um método relativamente simples e seguro o suficiente para ser usado à beira do leito. Cabe ser ressaltado que procedimentos à beira do leito são os mais adequados à logistica de uma unidade de suporte avançado, sobretudo quando se refere aos pacientes graves e instáveis, uma vez que a remoção dos mesmos aumenta em muito os riscos de complicações e intercorrências. Após o advento do cateter de artéria pulmonar, também conhecido como cateter de Swan-Ganz, surgiu o ramo da medicina intensiva que hoje é tema de muitos investimentos e discussões quanto ao seu real benefício pela comunidade científica, a monitorização hemodinâmica invasiva. O Dr Jeremy Swan faleceu em 2005 aos 82 anos de causas naturais. O Dr William Ganz faleceu em 2009 aos 90 anos, tambem de causas naturais. Consulte o Artigo Original no link abaixo: Referência: Swan HJC, Ganz W, Forrester J, Marcus 1L Diamond G, Chonette D. Catheterization of the heart in man with use of a flow directed balloon-tipped catheter, NEngl J Med 1970; 283: 447-451
|
AutoresGerenciado por: Arquivos
July 2012
Categorias
All
|
||||||||||||||||||||||||||||||||||||








 RSS Feed
RSS Feed

